Minťraux
Tableau 1. Composition moyenne de la croŻte
| …lťment (symbole) | % en poids |
| OxygŤne (O) | 46.6 |
| Silice (Si) | 27.7 |
| Aluminium (Al) | 8.1 |
| Fer (Fe) | 5.0 |
| Calcium (Ca) | 3.6 |
| Sodium (Na) | 2.8 |
| Potassium (K) | 2.6 |
| Magnťsium (Mg) | 2.1 |
| Total | 98.8 |

La plagioclase est un minťral commun dans les beaucoup de roche
volcanique. Photo
par „Steve
Mattox.
Un minťral , par dťfinition, doit satisfaire cinq conditions:
1. Il doit Ítre naturel.
2. Il doit Ítre inorganique.
3. Ce doit Ítre un ťlťment ou un composť plein.
4. Il doit avoir une composition dťfinie.
5. Il doit avoir une structure en cristal interne rťguliŤre.
Cette dťfinition exclue les milliers de composťs inventťs par des humains dans les laboratoires parce que ces composťs ne sont pas naturels. Des composťs qui sont trouvťs dans seulement des usines ou des animaux sont ťgalement exclus. Des liquides sont exclus parce qu'ils ne sont pas cristallins, leurs atomes sont libres pour se dťplacer. Les minerais peuvent Ítre un ťlťment simple, comme le diamant, qui est fait de carbone des composťs de deux ťlťments ou plus, comme le quartz, qui contient un silicium et deux atomes d'oxygŤne. La composition dťfinie indique qu'une analyse chimique d'un minťral donnť produira toujours le mÍme taux des ťlťments. Par exemple, le quartz aura toujours un silicium pour chaque deux atomes d'oxygŤne. Par consťquent, des minerais peuvent Ítre exprimťs par des formules chimiques, telles que SiO2 pour le quartz.
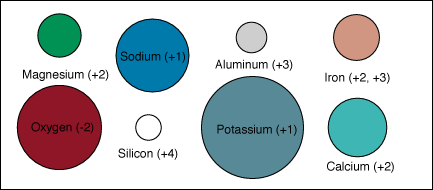
Ions communs dans les minťraux. Les tailles et les charges relatives sont indiquťes.
Dans certains minťraux, les ťlťments sont de taille et la charge semblable ils se remplacent l'un l'autre. La quantitť de fer et magnťsium dans l'olivine change de parce que ces ťlťments peuvent se remplacer l'un l'autre dans la structure du minťral. La formule pour l'olivine, (Mg, Fe)2SiO4, indique que pour chaque deux atomes de magnťsium et/ou de fer, il y a un atome de silicium et quatre atomes d'oxygŤne. La substitution du sodium pour le calcium se produit dans le plagioclase.
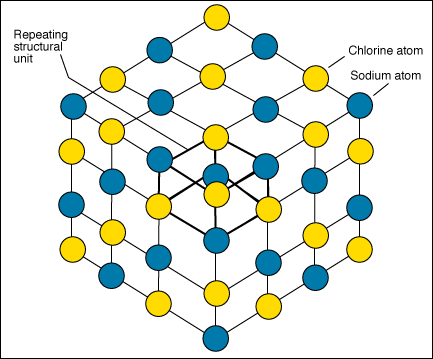
La structure cristalline interne rťguliŤre indique que les atomes sont arrangťs dans une configuration de rťpťtition rťguliŤre. Ce diagramme montre la structure de la halite. Des atomes le chlore et le sodium sont arrangťs dans une configuration de rťpťtition tridimensionnelle.
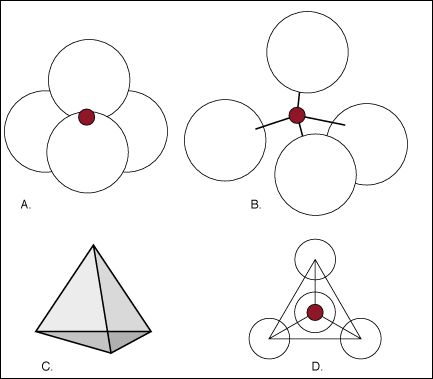
Un autre agencement de base, le tťtraŤdre de silice, se compose d'un atome de silicium entourť par quatre atomes d'oxygŤne aux coins du tťtraŤdre. Le tťtraŤdre de silice est une unitť de base de structure pour un groupe important de minťraux appelťs les silicates . Ce diagramme montre quatre reprťsentations du tťtraŤdre de silice.
A. L'oxygŤne est reprťsentť par les sphŤres
blanches et silicium par la sphŤre rouge plus petite.
B. Une vue augmentťe avec des tiges reprťsentant des liens entre les
atomes.
C. Reprťsentation schťmatique du tťtraŤdre, avec quatre points reprťsentant
les emplacements des atomes d'oxygŤne.
D. Reprťsentation schťmatique du tťtraŤdre regardant vers le bas d'en
haut.
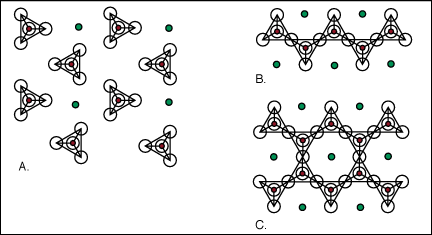
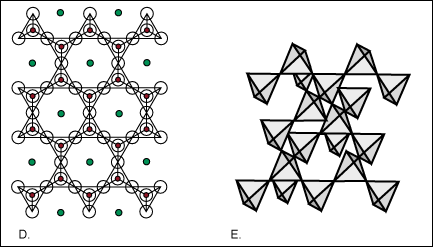
En mettent en commun les atomes d'oxygŤne adjacents, le tťtraŤdre peut former des chaÓnes, des feuilles, et des structures tridimensionnels.
A. La structure de l'olivine est basťe sur le tťtraŤdre
isolť de silice.
B. Les minťraux du pyroxŤne sont faits d'une chaÓne simple de tťtraŤdres.
C. Les minťraux d'amphibole sont faits d'une double chaÓne de tťtraŤdres.
D. Les micas, comme la biotite, sont des feuilles de tťtraŤdres.
E. Les structures de silicates , comme le plagioclase et le quartz,
sont les rťseaux tridimensionnels de tťtraŤdres de silice.
Tableau 2. Minerais communs dans la roche volcanique.
| Les minťraux de couleur clair (formule) | Minťraux colorťs (formule) | ||
| Feldspath: | Olivines | (Mg,Fe)2SiO4 | |
| Plagioclase | (Ca,Na)AlSi3O8 | PyroxŤnes | |
| Orthoclase | KAlSiO8 | HypersthŤne | (Mg,Fe)SiO3 |
| Anorthoclase | (K,Na)AlSi3O8 | Pigeonite | Ca(Mg, Fe) Si2O6 |
| Quartz | SiO2 | Augite | Ca(Mg,Fe)SiO6(Al, Fe)O3 |
| Nťphťline | NaAlSiO4 | Biotite | K(Mg, Fe)ŃlSiO10(OH)2 |
| Magnťtite | FeO4 | ||
| Hťmatite | Fe2O3 | ||